Mit der Veröffentlichung der Verordnung (EU) 2024/1860 am 9. Juli 2024 hat die EU eine schrittweise, modulweise Einführung von EUDAMED eingeführt. Zuvor waren die meisten Module nur auf freiwilliger Basis nutzbar, sollten jedoch verpflichtend werden, sobald sie funktionsfähig sind.
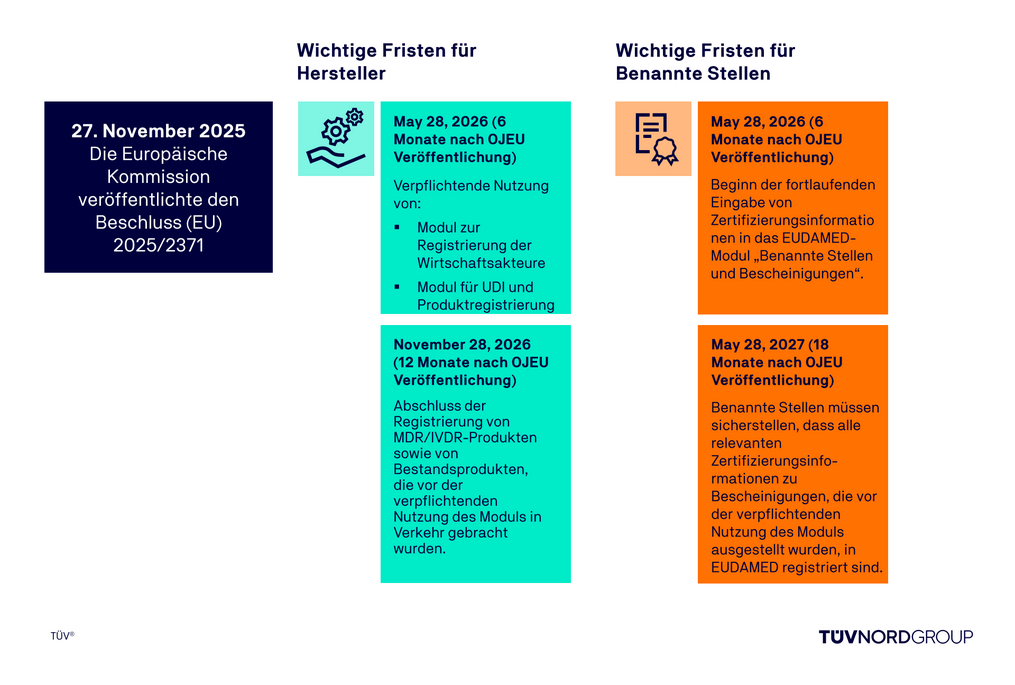
Am 27. November 2025 veröffentlichte die Europäische Kommission den Beschluss (EU) 2025/2371 und bestätigte, dass vier EUDAMED-Module nun vollständig funktionsfähig sind.
Diese Module sind:
1 Registrierung von Wirtschaftsakteuren (Actor registration )
2 UDI-/Produkt-Registrierung (Unique Device Identification (UDI) and device registration)
3 Benannte Stellen und Bescheinigungen (Notified Bodies and certificates)
6 Marktüberwachung (Market surveillance)
Mit dieser Veröffentlichung begann eine sechsmonatige Übergangsfrist, nach deren Ablauf diese vier Module ab dem 28. Mai 2026 verpflichtend werden.
Dies stellt einen wichtigen Meilenstein für Transparenz und Rückverfolgbarkeit von Produkten im EU-Regulierungsrahmen dar.